Apekopper: årsaker, symptomer, diagnose og behandling

Skrevet og verifisert av legen Leonardo Biolatto
Apekopper er i fokus for aktuelle helsenyheter rundt om i verden. Det er imidlertid ikke en ny sykdom. Faktisk er det rapportert om menneskelige tilfeller siden 1970-tallet.
Navnet kan virke forvirrende, og informasjonen som sirkulerer om det forårsaker også kontrovers. Hvordan overføres det mellom mennesker? Hvorfor gikk det fra å være en endemisk patologi i Kongo til å forårsake utbrudd i Europa, Amerika og Australia?
Siden 1980-tallet har tilfeller av apekopper blitt flere. Sakte, men jevnt og trutt. Vitenskapelige studier har fylt ut noen hull om viruset som forårsaker det, men det er fortsatt mange spørsmål.
I denne artikkelen vil vi forklare hva vi vet om sykdommen og de aller siste bevisene, i sammenheng med et utbrudd som Verdens helseorganisasjon (WHO) følger nøye med.
Hva er apekopper og hvordan oppsto det?
Apekopper hos mennesker ble først oppdaget i 1970. Pasient null var et barn i Den demokratiske republikken Kongo som hadde kopper-lignende vesikler, men som ikke oppfylte alle betingelsene for å bli erklært et tilfelle av den allerede kjente sykdommen.
Virusets reise startet imidlertid ikke der. Faktisk er den første vitenskapelige registreringen av dette koppeviruset hos primater, gjennom et utbrudd i laboratoriedyr, registrert i 1958.
Antistoffer mot det virale middelet ble senere isolert i gnagere og i aper av ulike arter med leveområder i Afrika. Imidlertid ble isolering av viruset som sådan, in vivo, bare oppnådd to ganger i den afrikanske skogen. Derfor vet vi ikke hva eller hvem det virkelige reservoaret er, dvs. hvor det finner en plass for å overleve og deretter forårsaker utbrudd.
Derfor er det riktig å si at vi har å gjøre med en zoonose. Dette er sykdommer som vanligvis overføres mellom visse dyr, men som av og til overføres til mennesker og kan (eller kanskje ikke) følge en påfølgende inter-menneskelig overføringsvei.
Denne gruppen av Orthopoxvirus er en del av Poxviridae-familien. Så langt er det 4 arter i denne kategorien som kan infisere mennesker:
- Koppevirus: Dette er det klassiske viruset kjent over hele verden som hadde en periode med intens spredning og deretter ble utryddet fra flere land.
- Vaccinia-virus: Dette er viruset som ble brukt til koppevaksinen. Det var nettopp denne enorme verdensomspennende vaksinasjonskampanjen som førte til erklæringen om utryddelse i ulike geografiske områder.
- Bovint koppevirus: Dette overføres fra landlige dyr, men dets oppførsel er assosiert med fangenskap, og det er også rapportert om menneskelige tilfeller fra dyreparker og sirkus.
- Apekopp-virus: Det vi har å gjøre med nå.
Overføring av apekopp-viruset
Zoonotisk overføring, dvs. fra dyr til mennesker, er den best dokumenterte overføringen om denne sykdommen. Og rapportene vi har kommer fra Afrika, landet hvor dette viruset nesten var begrenset til i flere tiår.
Selv om navnet apekopper antyder at ikke-menneskelige primater hovedsaklig er ansvarlige for overføringen til arten vår, er sannheten at forskning peker på gnagere. Inntak av gnagere i våre hjem, jakt for å utrydde dem som skadedyr, og håndtering av rotter og ekorn ser ut til å være det første kontaktpunktet for smitte.
I landlige områder i Afrika har de derfor identifisert situasjoner som gjør overføring fra dyr til mennesker mer sannsynlig. For eksempel når folk sover på bakken. Dette er også tilfelle hvis folk spiser ville dyr (nærmere bestemt gnagere).
Andre bevis har utelukket faktorer som kan betraktes som risikofaktorer, men som så langt ikke er det, for eksempel følgende:
- Å eie kjæledyr
- Å komme i kontakt med avføring fra ville dyr

Mellommenneskelig overføring
Det nåværende utbruddet av apekopper skyldes overføring mellom mennesker, siden de fjerne geografiske områdene og samtidigheten av tilfellene praktisk talt utelukker at de alle skyldes zoonotiske årsaker. Dette er ikke noe nytt, siden det ble oppdaget, har det vært rapporter om mellommenneskelige infeksjoner.
Det mest slående nå er kanskje antallet pasienter som utgjør smittekjeden. Selv med mennesker der selve kjeden ikke kan defineres; vi vet ikke hvordan de kan ha blitt smittet, og ingen av nærkontaktene deres har ingen symptomer.
I tidligere rapporter om utbrudd på 1980- og 1990-tallet nådde smittekjeden på det meste 8 personer. Dette det vil si ikke mer enn det antallet nære kontakter siden pasient null kunne bekreftes med en diagnose.
Dette representerer en svært lav angrepsrate sammenlignet med andre lignende sykdommer. Angrepsrate er et mål på epidemiologi for å bestemme hvor stor prosentandel av en pasients nærmeste kontakter som blir infisert av å bo eller tilbringe tid sammen.
Sammenlignet med klassiske kopper er dette ubetydelig, da sistnevnte har en angrepsrate på 80 %.
Selv om nærkontakt antas å være overføringsveien, er den mest spesifikke kjente ruten at overføring mellom mennesker vil komme fra luftbårne og kutane ruter, gjennom luftveisdråper og hud-mot-hud.
Som med vanlige kopper, er hudlesjoner og væsker som utskilles fra dem smittsomt. Viruset kan reise gjennom sekreter for å nå andre gjenstander og andre mennesker.
Den lave angrepsfrekvensen og mangelen på informasjon om overføringskjeden til det nåværende utbruddet tillater oss ikke å definere tydeligere omstendighetene som gjør smitte effektiv. Hvis det er en vanlig luftbåren rute (som influensa), hvorfor blir ikke flere nære kontakter av bekreftede pasienter smittet?
Et spesielt problem som diskuteres i det nåværende utbruddet er seksuell overføring. Det ser ut til å være en vanlig faktor blant pasienter der infeksjonskjeden er etablert. Men det er ingen bekreftelse, og noen spesialister anser det ikke engang som en mulig rute.
Finn ut mer: Les om de 5 vanligste seksuelt overførbare infeksjonene
Hva er symptomene på sykdommen?
Inkubasjonstiden for apekopper, dvs. tiden fra kontakt med viruset til de første symptomene oppstår, varierer fra 6 til 16 dager. Det er ikke helt klart, men 2 uker ser ut til å være gjennomsnittet.
De klassiske tilfellene begynner med feber som kan vare fra 1 til 4 dager. Det er ledsaget av de klassiske febersymptomene, med hodepine, tretthet, myalgi og somnolens.
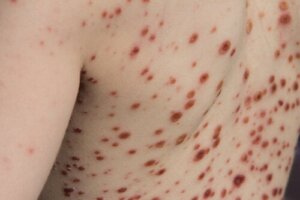
Så begynner det karakteristiske dermale utbruddet. Det som har blitt beskrevet så langt er en sentrifugal presentasjon (starter på kroppen og går videre til ekstremitetene) av makuler (flekker) og papler (hudforhøyelser), sammen med vesikler (med væskeinnhold) og pustler (med pussinnhold) som utvikler seg til skorper.
Betennelse i lymfeknuter er beryktet i tilfeller av apekopper. Dette skiller den fra klassiske kopper, som nesten ikke har lymfadenopati.
Alvorlighetsgraden er mild mesteparten av tiden, men den kan være dødelig i noen få tilfeller (1 % er dødeligheten i Afrika). Alvorlige tilfeller er ofte komplisert av oppkast og diaré, encefalitt og lungebetennelse. Noen av dem når sepsis og dør av multiorgansvikt.
Det er en reduksjon av pasientens immunrespons, noe som kan favorisere superinfeksjon med bakterier. Dette er en av forklaringene på de dødelige tilfellene som når sepsis.
Det er en spesiell situasjon hos gravide kvinner, fordi de gir høyere dødelighet og komplikasjoner når de er infisert med apekopper. På samme måte har noen rapporter bekreftet at det er vertikal overføring, det vil si fra mor til foster.
Identifisering av tilfeller
Gjennom historien, fra 1970 til nå, har det vært forskjellige definisjoner av mistenkte tilfeller av apekopper. Dette gjøres for å identifisere pasienter og isolere dem.
Hvert land etablerer varseltegn som vi bør være oppmerksomme på, og hvilke egenskaper helsesystemene skal reagere på. Men stort sett er det enighet om at en person mistenkes for å ha sykdommen når de har feber og vesikulært utslett, sammen med minst ett av følgende tre symptomer:
- Et utslett på håndflatene eller fotsålene.
- Betennelse i lymfeknuter.
- Episoder med forhøyet kroppstemperatur før utslettet vises.
Dette kommer selvsagt i tillegg til etterforskningen av hvem som var sammen med den mistenkte pasienten. Hvis personen med disse tegnene har vært i nærkontakt med noen som allerede har en bekreftet diagnose, øker sjansen for å være positiv.
Hvordan bekreftes diagnosen?
Det første trinnet på den diagnostiske veien for apekopper begynner med mistanke. Dette vil være de mistenkte tilfellene i henhold til definisjonen vi ga tidligere.
Disse pasientene må isoleres og testing må begynne for å avgjøre om patologien kan bekreftes eller ikke. Dette er ikke en rask løsning, siden det ennå ikke er et viralt middel som kan testes bredt over hele verden.
Flere steder har man valgt å be om IgG- og IgM-immunoglobulintesting mot Orthopoxvirus. Det er ikke spesifikt, men hvis resultatet er positivt, lar det bekreftelse fortsette, mens man venter på mer spesifikke resultater som kan ta litt tid.
Disse spesifikke testene avhenger av tilgjengeligheten ved hvert helsesenter:
- Polymerasekjedereaksjon (PCR)
- Immunhistokjemi
- Elektronmikroskopi
Disse metodene er kun tilgjengelige på enkelte plasser som mottar prøver fra andre geografiske områder. Derfor er forsinkelse nesten uunngåelig, og isolering av mistenkte bør brukes mens de venter.
Immunglobuliner, PCR og immunhistokjemi krever en blodprøve fra pasienten. Elektronmikroskopi brukes til å gjøre en visuell analyse av sekreter dersom sekret samles opp for å sendes til laboratoriet.
Hva er behandlingen av apekopper?
Apekopper har ingen konkret og spesifikk behandling. Som mange virale patologier, er det ikke noe spesielt medikament som kan blokkere eller avbryte replikasjonen av patogenet.
Derfor er det eksperter forfekter isolasjon med støttende tiltak. Noen pasienter med milde tilfeller krever ingen farmakologisk tilnærming. Andre er alvorlige nok til å berettige testing med antivirale midler.
Det er utilstrekkelig bevis på effektiviteten av antivirale midler for å redusere komplikasjoner. De er reservert for bruk etter behandlingsteamets skjønn hos de som forverres eller står i fare for å dø, det vil si hos 1 % av de diagnostiserte.
Brincidofovir og tecovirimat er navnene på to legemidler som har blitt studert for behandling av ortopoksvirus. De har fungert mer innen klassiske kopper, så i dag representerer de det beste alternativet for utbruddet.
På den annen side fortjener komplikasjoner sitt eget terapeutiske opplegg. Bakterielle superinfeksjoner, som er vanlige i alvorlige tilfeller, behandles med antibiotika spesifikke for mikroorganismen som er identifisert.
Ved lungebetennelser eller encefalitt som vises som en komplikasjon under sykehusinnleggelse, kan det medisinske teamet bestemme seg for å gi livsstøtte. Dette oppnås med assistert ventilasjon, dersom pasientens tilstand tilsier det. Det er ikke mye forskjellig fra det som er gjort med lignende tilstander forårsaket av andre etiologier.

Utskriving av pasienter
Det er fortsatt diskusjon om når pasienter skal skrives ut. De fleste kommer seg tilfredsstillende og har ingen følgetilstander. Men det er spørsmålet om overføring mellom mennesker som avgjør spørsmålet om når man skal la isolasjon ta slutt.
Ved tidligere utbrudd, både i Afrika og noen i USA og Storbritannia, ble det foreslått utskrivning når sårskorpene til pasientene forsvant. Det antas at personen på det tidspunktet ikke lenger er smittsom. Dette er tilfellet med klassiske kopper.
Noen pasienter har imidlertid vist seg å ha positive PCR-resultater i luftveiene inntil 3 uker etter at skorpene har forsvunnet. Det er ikke bekreftet om dette er synonymt med smittefare.
Også fra tidligere rapporter vet vi at det er pasienter som har lymfadenopati og hudutslett igjen etter samleie etter at de er utskrevet. Dette vekker mistanke om en forskansning av viruset i kjønnsområdet, noe som kan forlenge overføringen langs den ruten lenge etterpå.
Finnes det en vaksine?
US Food and Drug Administration (FDA) godkjente en vaksine kalt JYNNEOS i 2019. Denne immuniseringen vil være effektiv mot både kopper og apekopper.
Det er ikke bestemt at det skal være tilgjengelig for massemarkedsføring, selv om indikasjonen for risikopopulasjoner blir studert. Mennesker som bor i endemiske områder, nære kontakter med bekreftede tilfeller og arbeidere med eksponering for dyr som er kjent for å være reservoarer, kan være mottakere.
Vaksinasjonsskjemaet her er to doser med en måneds mellomrom, men vi understreker at det fortsatt ikke er noen godkjenning for inkludering i offisielle vaksinasjonsplaner eller for bruk under omstendighetene rundt dette nåværende utbruddet.
EU-landene jobber imidlertid med de juridiske spørsmålene for å skaffe doser og gi dem til nære kontakter, forutsatt at det kan produsere beskyttelse for å stoppe spredningen i utsatte grupper.
Det er kjent at de som er vaksinert med den klassiske koppevaksinen har en fordel. Beskyttelsen som gis av slik immunisering mot apekopper er beregnet til å være 85 %, noe som anses som mer enn akseptabelt.
En del av det unike med dette nåværende utbruddet skyldes faktisk at det er færre personer som er vaksinert med kopper på grunn av de geografiske områdene som er erklært utryddet. Dette vil ha økt følsomheten til populasjoner for virus fra samme familie.
Det nåværende utbruddet: hva vi vet
Det nåværende apekoppeutbruddet anses å ha startet 7. mai 2022, da Storbritannia rapporterte om et tilfelle utenfor Afrika. Til tross for dette foreslår noen epidemiologer å forlenge perioden fra 2021, da USA rapporterte om et lite antall tilfeller på sitt territorium.
Fra begynnelsen av mai til i dag er det mer enn 250 bekreftede tilfeller utenfor Afrika. Dette involverer 16 land.
Det er en enestående situasjon, spesielt med mer enn 100 mistenkte i isolasjon som venter på bekreftelse. Verdens helseorganisasjon har erklært utbruddet, men spesifiserer at det er mulig å kontrollere det. I tillegg til at risikoen for befolkningen generelt er lav.
I Spania er det 84 bekreftede tilfeller, Nord-Irland hadde sin første positive pasient 26. mai, det samme hadde Wales. Australia registrerte den første saken i Melbourne, i en person som returnerte fra Storbritannia.
Massachusetts-saken fra Montreal utløste et intensivt søk etter mistenkte i Canada, hvor 13 personer ble isolert. Samtidig hevet USA varslingsanbefalingen for internasjonale reiser, slik at ekstreme forholdsregler tas for å hindre smitte mellom mennesker.
Hva kan vi gjøre?
Forebyggende tiltak for å unngå å få apekopper har å gjøre med noen generelle retningslinjer og med restriksjoner som skal brukes under spesifikke omstendigheter. Blant de førstnevnte kan vi nevne følgende:
- Hyppig håndvask.
- Håndter mat av animalsk opprinnelse med maksimale sanitærtiltak.
- Kjøp kun matprodukter av animalsk opprinnelse på autoriserte steder og virksomheter.
- Når du reiser, opphold deg på steder som er sertifisert av helsemyndighetene og hvor skadedyrkontrollene som utføres i rommene er oversiktlige.
- Når du besøker naturreservater, som fornøyelsesparker eller dyreparker, må du ikke komme i kontakt med dyr og holde trygg avstand til dem.
Når det gjelder spesielle restriksjoner, skal det presiseres at en kontakt de siste 14-21 dagene med syke personer eller det faktum at man har reist til et geografisk område med utbrudd, innebærer at man bør konsultere helsemyndighetene. Isolering og screening med komplementære metoder bør utføres.
Selvisolering inntil konsultasjon er mulig bør være regelen for personer med disse egenskapene. På samme måte bør familiemedlemmer og samboere følge samme prosedyre inntil det er positiv eller negativ bekreftelse.
Det er viktig å ikke få panikk. Som Verdens helseorganisasjon har gjort klart, er vi ikke i en pandemisituasjon ennå, og det er ingen økt risiko for befolkningen generelt, så generelle hygienetiltak, tidlig identifisering av symptomer og konsultasjon i tvilstilfeller er tilstrekkelig.
Apekopper er i fokus for aktuelle helsenyheter rundt om i verden. Det er imidlertid ikke en ny sykdom. Faktisk er det rapportert om menneskelige tilfeller siden 1970-tallet.
Navnet kan virke forvirrende, og informasjonen som sirkulerer om det forårsaker også kontrovers. Hvordan overføres det mellom mennesker? Hvorfor gikk det fra å være en endemisk patologi i Kongo til å forårsake utbrudd i Europa, Amerika og Australia?
Siden 1980-tallet har tilfeller av apekopper blitt flere. Sakte, men jevnt og trutt. Vitenskapelige studier har fylt ut noen hull om viruset som forårsaker det, men det er fortsatt mange spørsmål.
I denne artikkelen vil vi forklare hva vi vet om sykdommen og de aller siste bevisene, i sammenheng med et utbrudd som Verdens helseorganisasjon (WHO) følger nøye med.
Hva er apekopper og hvordan oppsto det?
Apekopper hos mennesker ble først oppdaget i 1970. Pasient null var et barn i Den demokratiske republikken Kongo som hadde kopper-lignende vesikler, men som ikke oppfylte alle betingelsene for å bli erklært et tilfelle av den allerede kjente sykdommen.
Virusets reise startet imidlertid ikke der. Faktisk er den første vitenskapelige registreringen av dette koppeviruset hos primater, gjennom et utbrudd i laboratoriedyr, registrert i 1958.
Antistoffer mot det virale middelet ble senere isolert i gnagere og i aper av ulike arter med leveområder i Afrika. Imidlertid ble isolering av viruset som sådan, in vivo, bare oppnådd to ganger i den afrikanske skogen. Derfor vet vi ikke hva eller hvem det virkelige reservoaret er, dvs. hvor det finner en plass for å overleve og deretter forårsaker utbrudd.
Derfor er det riktig å si at vi har å gjøre med en zoonose. Dette er sykdommer som vanligvis overføres mellom visse dyr, men som av og til overføres til mennesker og kan (eller kanskje ikke) følge en påfølgende inter-menneskelig overføringsvei.
Denne gruppen av Orthopoxvirus er en del av Poxviridae-familien. Så langt er det 4 arter i denne kategorien som kan infisere mennesker:
- Koppevirus: Dette er det klassiske viruset kjent over hele verden som hadde en periode med intens spredning og deretter ble utryddet fra flere land.
- Vaccinia-virus: Dette er viruset som ble brukt til koppevaksinen. Det var nettopp denne enorme verdensomspennende vaksinasjonskampanjen som førte til erklæringen om utryddelse i ulike geografiske områder.
- Bovint koppevirus: Dette overføres fra landlige dyr, men dets oppførsel er assosiert med fangenskap, og det er også rapportert om menneskelige tilfeller fra dyreparker og sirkus.
- Apekopp-virus: Det vi har å gjøre med nå.
Overføring av apekopp-viruset
Zoonotisk overføring, dvs. fra dyr til mennesker, er den best dokumenterte overføringen om denne sykdommen. Og rapportene vi har kommer fra Afrika, landet hvor dette viruset nesten var begrenset til i flere tiår.
Selv om navnet apekopper antyder at ikke-menneskelige primater hovedsaklig er ansvarlige for overføringen til arten vår, er sannheten at forskning peker på gnagere. Inntak av gnagere i våre hjem, jakt for å utrydde dem som skadedyr, og håndtering av rotter og ekorn ser ut til å være det første kontaktpunktet for smitte.
I landlige områder i Afrika har de derfor identifisert situasjoner som gjør overføring fra dyr til mennesker mer sannsynlig. For eksempel når folk sover på bakken. Dette er også tilfelle hvis folk spiser ville dyr (nærmere bestemt gnagere).
Andre bevis har utelukket faktorer som kan betraktes som risikofaktorer, men som så langt ikke er det, for eksempel følgende:
- Å eie kjæledyr
- Å komme i kontakt med avføring fra ville dyr

Mellommenneskelig overføring
Det nåværende utbruddet av apekopper skyldes overføring mellom mennesker, siden de fjerne geografiske områdene og samtidigheten av tilfellene praktisk talt utelukker at de alle skyldes zoonotiske årsaker. Dette er ikke noe nytt, siden det ble oppdaget, har det vært rapporter om mellommenneskelige infeksjoner.
Det mest slående nå er kanskje antallet pasienter som utgjør smittekjeden. Selv med mennesker der selve kjeden ikke kan defineres; vi vet ikke hvordan de kan ha blitt smittet, og ingen av nærkontaktene deres har ingen symptomer.
I tidligere rapporter om utbrudd på 1980- og 1990-tallet nådde smittekjeden på det meste 8 personer. Dette det vil si ikke mer enn det antallet nære kontakter siden pasient null kunne bekreftes med en diagnose.
Dette representerer en svært lav angrepsrate sammenlignet med andre lignende sykdommer. Angrepsrate er et mål på epidemiologi for å bestemme hvor stor prosentandel av en pasients nærmeste kontakter som blir infisert av å bo eller tilbringe tid sammen.
Sammenlignet med klassiske kopper er dette ubetydelig, da sistnevnte har en angrepsrate på 80 %.
Selv om nærkontakt antas å være overføringsveien, er den mest spesifikke kjente ruten at overføring mellom mennesker vil komme fra luftbårne og kutane ruter, gjennom luftveisdråper og hud-mot-hud.
Som med vanlige kopper, er hudlesjoner og væsker som utskilles fra dem smittsomt. Viruset kan reise gjennom sekreter for å nå andre gjenstander og andre mennesker.
Den lave angrepsfrekvensen og mangelen på informasjon om overføringskjeden til det nåværende utbruddet tillater oss ikke å definere tydeligere omstendighetene som gjør smitte effektiv. Hvis det er en vanlig luftbåren rute (som influensa), hvorfor blir ikke flere nære kontakter av bekreftede pasienter smittet?
Et spesielt problem som diskuteres i det nåværende utbruddet er seksuell overføring. Det ser ut til å være en vanlig faktor blant pasienter der infeksjonskjeden er etablert. Men det er ingen bekreftelse, og noen spesialister anser det ikke engang som en mulig rute.
Finn ut mer: Les om de 5 vanligste seksuelt overførbare infeksjonene
Hva er symptomene på sykdommen?
Inkubasjonstiden for apekopper, dvs. tiden fra kontakt med viruset til de første symptomene oppstår, varierer fra 6 til 16 dager. Det er ikke helt klart, men 2 uker ser ut til å være gjennomsnittet.
De klassiske tilfellene begynner med feber som kan vare fra 1 til 4 dager. Det er ledsaget av de klassiske febersymptomene, med hodepine, tretthet, myalgi og somnolens.
Så begynner det karakteristiske dermale utbruddet. Det som har blitt beskrevet så langt er en sentrifugal presentasjon (starter på kroppen og går videre til ekstremitetene) av makuler (flekker) og papler (hudforhøyelser), sammen med vesikler (med væskeinnhold) og pustler (med pussinnhold) som utvikler seg til skorper.
Betennelse i lymfeknuter er beryktet i tilfeller av apekopper. Dette skiller den fra klassiske kopper, som nesten ikke har lymfadenopati.
Alvorlighetsgraden er mild mesteparten av tiden, men den kan være dødelig i noen få tilfeller (1 % er dødeligheten i Afrika). Alvorlige tilfeller er ofte komplisert av oppkast og diaré, encefalitt og lungebetennelse. Noen av dem når sepsis og dør av multiorgansvikt.
Det er en reduksjon av pasientens immunrespons, noe som kan favorisere superinfeksjon med bakterier. Dette er en av forklaringene på de dødelige tilfellene som når sepsis.
Det er en spesiell situasjon hos gravide kvinner, fordi de gir høyere dødelighet og komplikasjoner når de er infisert med apekopper. På samme måte har noen rapporter bekreftet at det er vertikal overføring, det vil si fra mor til foster.
Identifisering av tilfeller
Gjennom historien, fra 1970 til nå, har det vært forskjellige definisjoner av mistenkte tilfeller av apekopper. Dette gjøres for å identifisere pasienter og isolere dem.
Hvert land etablerer varseltegn som vi bør være oppmerksomme på, og hvilke egenskaper helsesystemene skal reagere på. Men stort sett er det enighet om at en person mistenkes for å ha sykdommen når de har feber og vesikulært utslett, sammen med minst ett av følgende tre symptomer:
- Et utslett på håndflatene eller fotsålene.
- Betennelse i lymfeknuter.
- Episoder med forhøyet kroppstemperatur før utslettet vises.
Dette kommer selvsagt i tillegg til etterforskningen av hvem som var sammen med den mistenkte pasienten. Hvis personen med disse tegnene har vært i nærkontakt med noen som allerede har en bekreftet diagnose, øker sjansen for å være positiv.
Hvordan bekreftes diagnosen?
Det første trinnet på den diagnostiske veien for apekopper begynner med mistanke. Dette vil være de mistenkte tilfellene i henhold til definisjonen vi ga tidligere.
Disse pasientene må isoleres og testing må begynne for å avgjøre om patologien kan bekreftes eller ikke. Dette er ikke en rask løsning, siden det ennå ikke er et viralt middel som kan testes bredt over hele verden.
Flere steder har man valgt å be om IgG- og IgM-immunoglobulintesting mot Orthopoxvirus. Det er ikke spesifikt, men hvis resultatet er positivt, lar det bekreftelse fortsette, mens man venter på mer spesifikke resultater som kan ta litt tid.
Disse spesifikke testene avhenger av tilgjengeligheten ved hvert helsesenter:
- Polymerasekjedereaksjon (PCR)
- Immunhistokjemi
- Elektronmikroskopi
Disse metodene er kun tilgjengelige på enkelte plasser som mottar prøver fra andre geografiske områder. Derfor er forsinkelse nesten uunngåelig, og isolering av mistenkte bør brukes mens de venter.
Immunglobuliner, PCR og immunhistokjemi krever en blodprøve fra pasienten. Elektronmikroskopi brukes til å gjøre en visuell analyse av sekreter dersom sekret samles opp for å sendes til laboratoriet.
Hva er behandlingen av apekopper?
Apekopper har ingen konkret og spesifikk behandling. Som mange virale patologier, er det ikke noe spesielt medikament som kan blokkere eller avbryte replikasjonen av patogenet.
Derfor er det eksperter forfekter isolasjon med støttende tiltak. Noen pasienter med milde tilfeller krever ingen farmakologisk tilnærming. Andre er alvorlige nok til å berettige testing med antivirale midler.
Det er utilstrekkelig bevis på effektiviteten av antivirale midler for å redusere komplikasjoner. De er reservert for bruk etter behandlingsteamets skjønn hos de som forverres eller står i fare for å dø, det vil si hos 1 % av de diagnostiserte.
Brincidofovir og tecovirimat er navnene på to legemidler som har blitt studert for behandling av ortopoksvirus. De har fungert mer innen klassiske kopper, så i dag representerer de det beste alternativet for utbruddet.
På den annen side fortjener komplikasjoner sitt eget terapeutiske opplegg. Bakterielle superinfeksjoner, som er vanlige i alvorlige tilfeller, behandles med antibiotika spesifikke for mikroorganismen som er identifisert.
Ved lungebetennelser eller encefalitt som vises som en komplikasjon under sykehusinnleggelse, kan det medisinske teamet bestemme seg for å gi livsstøtte. Dette oppnås med assistert ventilasjon, dersom pasientens tilstand tilsier det. Det er ikke mye forskjellig fra det som er gjort med lignende tilstander forårsaket av andre etiologier.

Utskriving av pasienter
Det er fortsatt diskusjon om når pasienter skal skrives ut. De fleste kommer seg tilfredsstillende og har ingen følgetilstander. Men det er spørsmålet om overføring mellom mennesker som avgjør spørsmålet om når man skal la isolasjon ta slutt.
Ved tidligere utbrudd, både i Afrika og noen i USA og Storbritannia, ble det foreslått utskrivning når sårskorpene til pasientene forsvant. Det antas at personen på det tidspunktet ikke lenger er smittsom. Dette er tilfellet med klassiske kopper.
Noen pasienter har imidlertid vist seg å ha positive PCR-resultater i luftveiene inntil 3 uker etter at skorpene har forsvunnet. Det er ikke bekreftet om dette er synonymt med smittefare.
Også fra tidligere rapporter vet vi at det er pasienter som har lymfadenopati og hudutslett igjen etter samleie etter at de er utskrevet. Dette vekker mistanke om en forskansning av viruset i kjønnsområdet, noe som kan forlenge overføringen langs den ruten lenge etterpå.
Finnes det en vaksine?
US Food and Drug Administration (FDA) godkjente en vaksine kalt JYNNEOS i 2019. Denne immuniseringen vil være effektiv mot både kopper og apekopper.
Det er ikke bestemt at det skal være tilgjengelig for massemarkedsføring, selv om indikasjonen for risikopopulasjoner blir studert. Mennesker som bor i endemiske områder, nære kontakter med bekreftede tilfeller og arbeidere med eksponering for dyr som er kjent for å være reservoarer, kan være mottakere.
Vaksinasjonsskjemaet her er to doser med en måneds mellomrom, men vi understreker at det fortsatt ikke er noen godkjenning for inkludering i offisielle vaksinasjonsplaner eller for bruk under omstendighetene rundt dette nåværende utbruddet.
EU-landene jobber imidlertid med de juridiske spørsmålene for å skaffe doser og gi dem til nære kontakter, forutsatt at det kan produsere beskyttelse for å stoppe spredningen i utsatte grupper.
Det er kjent at de som er vaksinert med den klassiske koppevaksinen har en fordel. Beskyttelsen som gis av slik immunisering mot apekopper er beregnet til å være 85 %, noe som anses som mer enn akseptabelt.
En del av det unike med dette nåværende utbruddet skyldes faktisk at det er færre personer som er vaksinert med kopper på grunn av de geografiske områdene som er erklært utryddet. Dette vil ha økt følsomheten til populasjoner for virus fra samme familie.
Det nåværende utbruddet: hva vi vet
Det nåværende apekoppeutbruddet anses å ha startet 7. mai 2022, da Storbritannia rapporterte om et tilfelle utenfor Afrika. Til tross for dette foreslår noen epidemiologer å forlenge perioden fra 2021, da USA rapporterte om et lite antall tilfeller på sitt territorium.
Fra begynnelsen av mai til i dag er det mer enn 250 bekreftede tilfeller utenfor Afrika. Dette involverer 16 land.
Det er en enestående situasjon, spesielt med mer enn 100 mistenkte i isolasjon som venter på bekreftelse. Verdens helseorganisasjon har erklært utbruddet, men spesifiserer at det er mulig å kontrollere det. I tillegg til at risikoen for befolkningen generelt er lav.
I Spania er det 84 bekreftede tilfeller, Nord-Irland hadde sin første positive pasient 26. mai, det samme hadde Wales. Australia registrerte den første saken i Melbourne, i en person som returnerte fra Storbritannia.
Massachusetts-saken fra Montreal utløste et intensivt søk etter mistenkte i Canada, hvor 13 personer ble isolert. Samtidig hevet USA varslingsanbefalingen for internasjonale reiser, slik at ekstreme forholdsregler tas for å hindre smitte mellom mennesker.
Hva kan vi gjøre?
Forebyggende tiltak for å unngå å få apekopper har å gjøre med noen generelle retningslinjer og med restriksjoner som skal brukes under spesifikke omstendigheter. Blant de førstnevnte kan vi nevne følgende:
- Hyppig håndvask.
- Håndter mat av animalsk opprinnelse med maksimale sanitærtiltak.
- Kjøp kun matprodukter av animalsk opprinnelse på autoriserte steder og virksomheter.
- Når du reiser, opphold deg på steder som er sertifisert av helsemyndighetene og hvor skadedyrkontrollene som utføres i rommene er oversiktlige.
- Når du besøker naturreservater, som fornøyelsesparker eller dyreparker, må du ikke komme i kontakt med dyr og holde trygg avstand til dem.
Når det gjelder spesielle restriksjoner, skal det presiseres at en kontakt de siste 14-21 dagene med syke personer eller det faktum at man har reist til et geografisk område med utbrudd, innebærer at man bør konsultere helsemyndighetene. Isolering og screening med komplementære metoder bør utføres.
Selvisolering inntil konsultasjon er mulig bør være regelen for personer med disse egenskapene. På samme måte bør familiemedlemmer og samboere følge samme prosedyre inntil det er positiv eller negativ bekreftelse.
Det er viktig å ikke få panikk. Som Verdens helseorganisasjon har gjort klart, er vi ikke i en pandemisituasjon ennå, og det er ingen økt risiko for befolkningen generelt, så generelle hygienetiltak, tidlig identifisering av symptomer og konsultasjon i tvilstilfeller er tilstrekkelig.
Alle siterte kilder ble grundig gjennomgått av teamet vårt for å sikre deres kvalitet, pålitelighet, aktualitet og validitet. Bibliografien i denne artikkelen ble betraktet som pålitelig og av akademisk eller vitenskapelig nøyaktighet.
- Marennikova SS, Seluhina EM, Malceva NM, Ladnyj ID. Poxviruses isolated from clinically ill and asymptomalically infected monkeys and a chimpanzee. Bulletin of the World Health Organization. 1972;46(5):613–20. pmid:4340220.
- Doty JB, Malekani JM, Kalemba LN, Stanley WT, Monroe BP, Nakazawa YU, et al. Assessing Monkeypox Virus Prevalence in Small Mammals at the Human-Animal Interface in the Democratic Republic of the Congo. Viruses. 2017;9(10):03. pmid:28972544.
- Ogoina D, Iroezindu M, James HI, Oladokun R, Yinka-Ogunleye A, Wakama P, Otike-Odibi B, Usman LM, Obazee E, Aruna O, Ihekweazu C. Clinical course and outcome of human monkeypox in Nigeria. Clinical Infectious Diseases. 2020 Oct 15;71(8):e210-4.
- Coto, C. E. (2009). Virus sin fronteras: el caso del virus cow pox, agente de la viruela bovina. Química Viva, 8(2), 57-63.
- Reynolds MG, Carroll DS, Olson VA, Hughes C, Galley J, Likos A, et al. A silent enzootic of an orthopoxvirus in Ghana, West Africa: Evidence for multi-species involvement in the absence of widespread human disease. American Journal of Tropical Medicine and Hygiene. 2010;82(4):746–54. pmid:20348530
- Mbala PK, Huggins JW, Riu-Rovira T, Ahuka SM, Mulembakani P, Rimoin AW, et al. Maternal and Fetal Outcomes among Pregnant Women with Human Monkeypox Infection in the Democratic Republic of Congo. Journal of Infectious Diseases. 2017;216(7):824–8. pmid:29029147.
- Jezek Z, Grab B, Szczeniowski M, Paluku KM, Mutombo M. Clinico-epidemiological features of monkeypox patients with an animal or human source of infection. Bulletin of the World Health Organization. 1988;66(4):459–64. pmid:2844428
- Nolen LD, Osadebe L, Katomba J, Likofata J, Mukadi D, Monroe B, Doty J, Hughes CM, Kabamba J, Malekani J, Bomponda PL, Lokota JI, Balilo MP, Likafi T, Lushima RS, Ilunga BK, Nkawa F, Pukuta E, Karhemere S, Tamfum JJ, Nguete B, Wemakoy EO, McCollum AM, Reynolds MG. Extended Human-to-Human Transmission during a Monkeypox Outbreak in the Democratic Republic of the Congo. Emerg Infect Dis. 2016 Jun;22(6):1014-21. doi: 10.3201/eid2206.150579. Erratum in: Emerg Infect Dis. 2016 Oct;22(10 ): PMID: 27191380; PMCID: PMC4880088.
- Reynolds, M. G., Yorita, K. L., Kuehnert, M. J., Davidson, W. B., Huhn, G. D., Holman, R. C., & Damon, I. K. (2006). Clinical manifestations of human monkeypox influenced by route of infection. The Journal of infectious diseases, 194(6), 773-780.
- Mwanbal, P. T., Tshioko, K. F., Moudi, A., Mukinda, V., Mwema, G. N., Messinger, D., … & Esposito, J. J. (1997). Casos humanos de viruela de los monos en Kasai Oriental, Zaire (1996-1997). Eurosurveillance, 2(5), 33-35.
- Chittick G, Morrison M, Brundage T, Nichols WG. Short-term clinical safety profile of brincidofovir: A favorable benefit–risk proposition in the treatment of smallpox. Antiviral research. 2017 Jul 1;143:269-77.
- Grosenbach DW, Honeychurch K, Rose EA, Chinsangaram J, Frimm A, Maiti B, Lovejoy C, Meara I, Long P, Hruby DE. Oral tecovirimat for the treatment of smallpox. New England Journal of Medicine. 2018 Jul 5;379(1):44-53.
- Reynolds MG, Davidson WB, Curns AT, Conover CS, Huhn G, Davis JP, et al. Spectrum of infection and risk factors for human monkeypox, United States, 2003. Emerging Infectious Diseases. 2007;13(9):1332–9. pmid:18252104.
- Panning M, Asper M, Kramme S, Schmitz H, Drosten C. Rapid detection and differentiation of human pathogenic orthopox viruses by a fluorescence resonance energy transfer real-time PCR assay. Clinical Chemistry. 2004;50(4):702–8. pmid:14962998.
Denne teksten tilbys kun til informasjonsformål og erstatter ikke konsultasjon med en profesjonell. Ved tvil, konsulter din spesialist.








